Estados alotrópicos
Se conocen cinco formas alotrópicas del carbono, además del amorfo: grafito, diamante, fullereno, grafeno y carbino.
Una de las formas en las cuales se encuentra el carbono es el grafito, caracterizado por tener sus átomos "en los vértices de hexágonos que tapizan un plano", es de color negro, opaco y blando, y es el material del cual está hecha la parte interior de los lápices de madera comúnmente conocida como mina. El grafito tiene exactamente los mismos átomos del diamante, pero por estar dispuestos en diferente forma tienen distintas propiedades físicas y químicas. Los diamantes naturales se forman en lugares donde el carbono ha sido sometido a grandes presiones y altas temperaturas. Su estructura es tetraédrica, lo que genera una red tridimensional y, a diferencia del grafito, tiene un grado de dureza alto: 10 Mohs. Los diamantes se pueden crear artificialmente, sometiendo el grafito a temperaturas y presiones muy altas. El precio del grafito es menor al de los diamantes naturales, pero si se han elaborado adecuadamente tienen la misma dureza, color y transparencia.

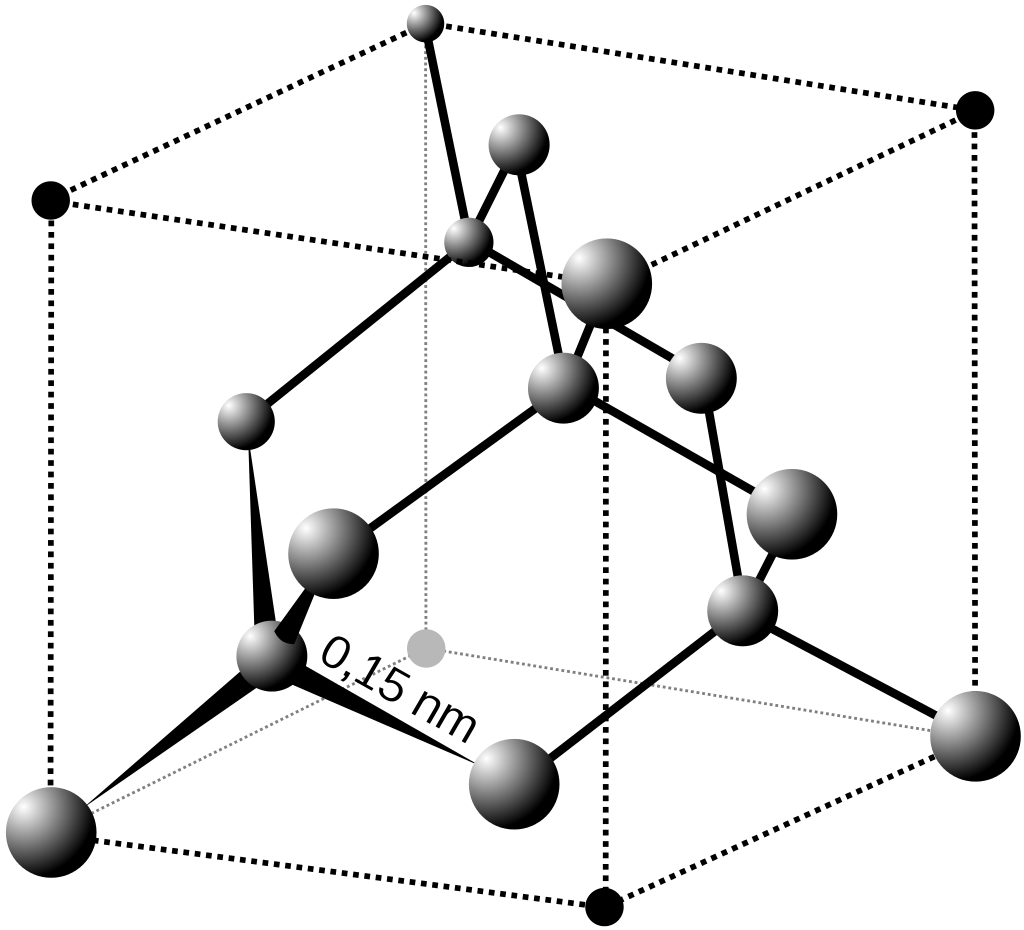
Fig.1. Estructuras del grafito y el diamante, respectivamente.
La forma amorfa es esencialmente grafito, pero no llega a adoptar una estructura cristalina macroscópica. Esta es la forma presente en la mayoría de los carbones y en el hollín.
A presión normal, el carbono adopta la forma del grafito, en la que cada átomo está unido a otros tres en un plano compuesto de celdas hexagonales; este estado se puede describir como tres electrones de valencia en orbitales híbridos planos sp² y el cuarto en el orbital p.
Las dos formas de grafito conocidas alfa (hexagonal) y beta (romboédrica) tienen propiedades físicas idénticas. Los grafitos naturales contienen más del 30 % de la forma beta, mientras que el grafito sintético contiene únicamente la forma alfa. La forma alfa puede transformarse en beta mediante procedimientos mecánicos, y esta recristalizar en forma alfa al calentarse por encima de 1000 °C.
Debido a la deslocalización de los electrones del orbital pi, el grafito es conductor de la electricidad, propiedad que permite su uso en procesos de electroerosión. El material es blando y las diferentes capas, a menudo separadas por átomos intercalados, se encuentran unidas por enlaces de Van de Waals, siendo relativamente fácil que unas deslicen respecto de otras, lo que le da utilidad como lubricante.
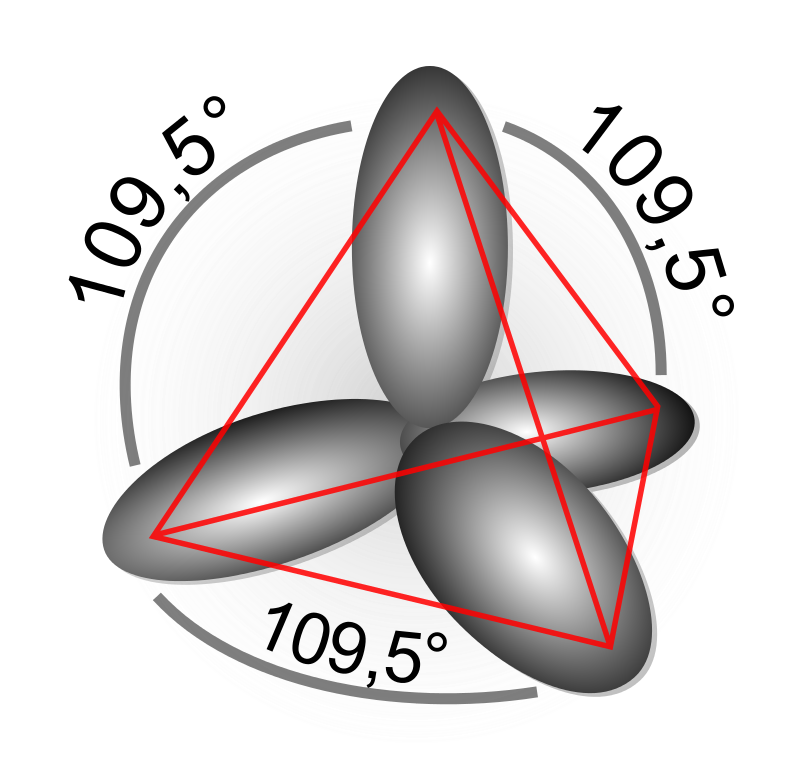
A muy altas presiones, el carbono adopta la forma del diamante, en el cual cada átomo está unido a otros cuatro átomos de carbono, encontrándose los 4 electrones en orbitales sp³, como en los hidrocarburos. El diamante presenta la misma estructura cúbica que el silicio y el germanio y, gracias a la resistencia del enlace químico carbono-carbono, es, junto con el nitruro de boro, la sustancia más dura conocida. La transición a grafito a temperatura ambiente es tan lenta que es indetectable. Bajo ciertas condiciones, el carbono cristaliza como lonsdaleíta, una forma similar al diamante pero hexagonal.
El orbital híbrido sp1 que forma enlaces covalentes solo es de interés en química, manifestándose en algunos compuestos, como por ejemplo el acetileno.
Los fullerenos fueron descubiertos hace 15 años tienen una estructura similar al grafito, pero el empaquetamiento hexagonal se combina con pentágonos (y en ciertos casos, heptágonos), lo que curva los planos y permite la aparición de estructuras de forma esférica, elipsoidal o cilíndrica. El constituido por 60 átomos de carbono, que presenta una estructura tridimensional y geometría similar a un balón de fútbol, es especialmente estable. Los fullerenos en general, y los derivados del C60 en particular, son objeto de intensa investigación en química desde su descubrimiento a mediados de los 1980.

A esta familia pertenecen también los nanotubos de carbono, que pueden describirse como capas de grafito enrolladas en forma cilíndrica y rematadas en sus extremos por hemiesferas (fulerenos), y que constituyen uno de los primeros productos industriales de la nanotecnología.