Al principio del curso estudiamos que la Química es la ciencia que se encargaba de estudiar la estructura de la materia y las transformaciones que ésta podía sufrir. Así, decíamos que un proceso químico tenía lugar siempre que unas sustancias se transformaban en otras sustancias diferentes. A las sustancias iniciales se les llama reactivos, y a las nuevas sustancias que se obtienen, productos. Aunque estamos rodeados de reacciones químicas (por ejemplo, en nuestro organismo tienen lugar miles de ellas), no se pudo explicar cómo tenían lugar hasta que no se descubrió la estructura interna de la materia. Podemos estudiar cómo tiene lugar una reacción química de 2 maneras o puntos de vista diferentes:
1. Punto de vista macroscópico: A simple vista, observamos que una reacción química tiene lugar siempre que, al poner en contacto 2 o más sustancias, o a partir de una única sustancia, se obtienen al cabo de un cierto tiempo una o varias sustancias totalmente diferentes de las iniciales. Es lo que sucede, por ejemplo, cuando quemamos un trozo de papel: al cabo del tiempo aparece una nueva sustancia, la ceniza. Podemos saber cuándo ha tenido lugar una reacción cuando...
• ...se produce una precipitación, es decir, se obtiene una sustancia insoluble y que se queda en el fondo del recipiente.
• ...se produce un desprendimiento de gases (burbujas si el gas está disuelto en agua).
• ...cambia la temperatura, pues en todas las reacciones químicas se absorbe calor (reacciones endotérmicas) o se desprende (reacciones exotérmicas).
• ...se produce un cambio de color, siempre que alguno de los productos tenga un color diferente al de los reactivos.
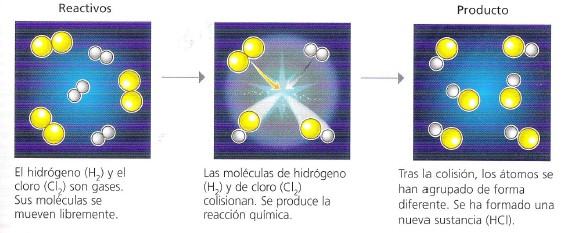
2. Punto de vista microscópico: Sabemos que cualquier sustancia está formada por átomos, los cuales se unen entre sí para dar lugar a los distintos compuestos químicos. Cuando dos o más sustancias reaccionan, lo
que sucede es que los átomos que forman parte de las sustancias iniciales se reordenan de forma diferente, de manera que aparecerán nuevas sustancias. Así, desde el punto de vista microscópico, una reacción química
no es más que una reordenación de los átomos que forman parte de los reactivos, obteniéndose entonces unas nuevas sustancias (los productos). Esta reordenación suele tener lugar debido a las colisiones de los átomos
entre sí (siempre que tengan lugar a elevadas energías), y generalmente se ve favorecida si aumenta la temperatura o la concentración de los reactivos.
Para representar de forma abreviada toda la información relacionada con una determinada reacción química se utilizan las ecuaciones químicas. En ellas, los reactivos y los productos se escriben mediante sus
fórmulas correspondientes, separados con una flecha que indica el sentido de la reacción (y que separa los dos miembros de la ecuación). Si hay varios reactivos (o productos) se separan con el signo “+”. Asimismo,
al lado de cada compuesto puede representarse abreviadamente el estado de agregación en que se encuentra:
s: estado sólido l: estado líquido g: estado gaseoso ac: disuelto en agua