 Fue establecida en el año 1789 por el químico francés Antoine Laurent Lavoisier, y establece lo siguiente:
Fue establecida en el año 1789 por el químico francés Antoine Laurent Lavoisier, y establece lo siguiente:
| En toda reacción química la masa se conserva, es decir, la masa total de los reactivos es igual a la masa total de los productos. |
La ley anterior implica que el número de átomos de cada elemento químico en ambos miembros de la reacción debe ser siempre el mismo (pues, como antes hemos dicho, una reacción química no es más que un reajuste o reordenación de átomos). Para conseguirlo, debemos ajustar la reacción, escribiendo delante de las fórmulas unos números, llamados coeficientes estequiométricos, que nos indican el número de átomos o moléculas que intervienen en la reacción. Así pues, cuando la ecuación química está ajustada podemos conocer...
• ...los reactivos y productos que participan en ella.
• ...el número de partículas (átomos o moléculas) que interviene de cada sustancia, ya sea un reactivo o un producto.
Cuando ajustemos una ecuación química procuraremos que los coeficientes estequiométricos sean los más sencillos posibles. Haremos el ajuste por tanteo, es decir, probando los coeficientes estequiométricos hasta que demos con aquellos que hagan que se cumpla la ley de conservación de la masa (mismo nº de átomos de cada elemento químico en ambos miembros de la ecuación química). Mostramos a continuación algunos ejemplos de ecuaciones químicas ajustadas. Observar que en todas ellas se conserva la masa, es decir, las masas de reactivos y productos son siempre iguales:

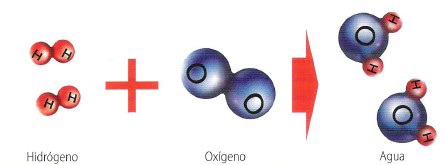
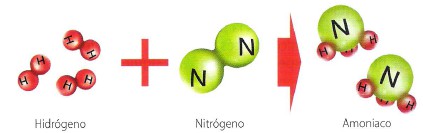
2 H2 + O2 → H2O 3 H2 + N2 → 2 NH3
A continuación, se muestra un vídeo explicativo para el ajuste de las reacciones químicas: